Будьте уверены
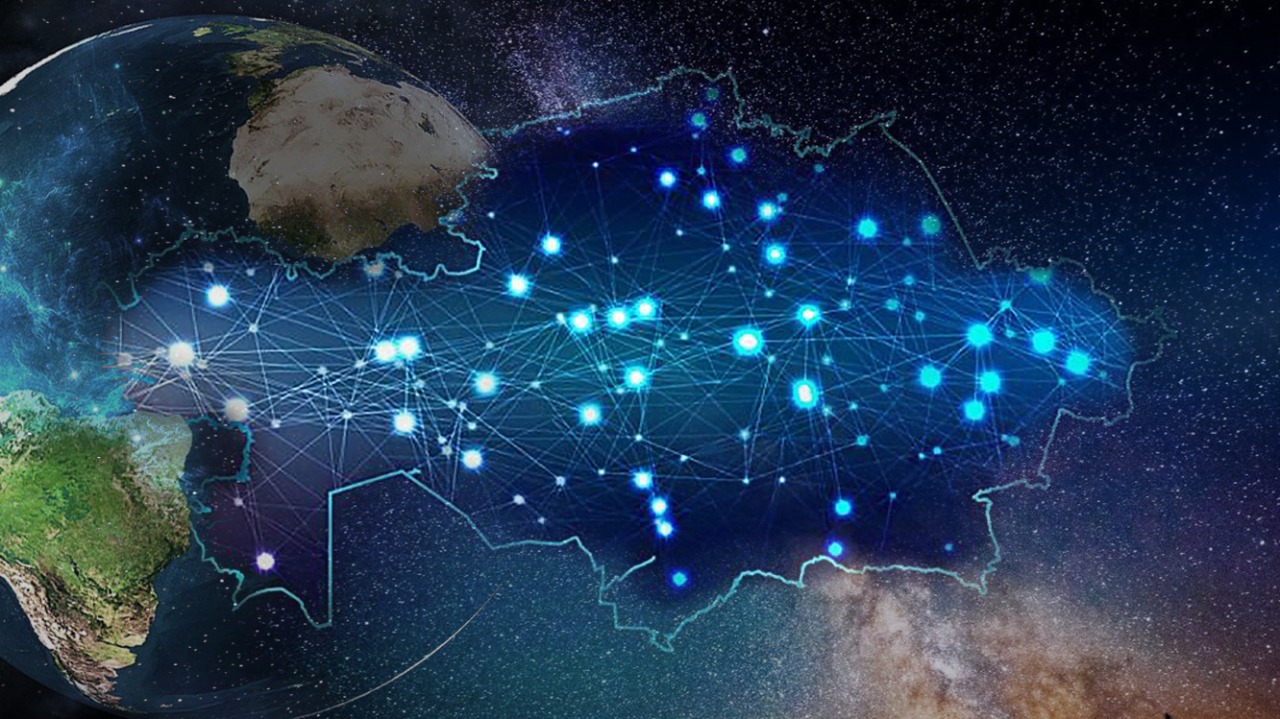 Фото - Тахир САСЫКОВ
Фото - Тахир САСЫКОВ
|
Насколько компетентно проверяются все поступающие на рынок страны фармпрепараты? Специалисты испытательной лаборатории Национального центра экспертизы лекарственных средств, изделий медицинского назначения и медицинской техники (НЦЭЛС) МЗСР РК в Алматы провели экскурсию для журналистов по своим лабораториям. |
На вопрос, что ждет казахстанский рынок лекарственных средств при объединении его с рынками стран Евразийского экономического союза, ответила директор испытательного центра НЦЭЛС Гульзада ЖУНУСОВА.
По последнему слову техники
– Казахстан в этой части опережает многих своих партнеров по союзу, даже в какой-то части и Россию. Потому что у нас есть своя государственная фармакопея (свод обязательных правил, которыми руководствуются при изготовлении, проверке, хранении и прописке больным лекарственных препаратов). Заведены такие фармакопейные пределы, ниже уровня которых завозить лекарства нельзя. Не во всех странах бывшего СНГ имеются такие ограничения. Таковых нет, например, в Киргизии и Узбекистане…
– Наш испытательный центр, – продолжает Гульзада Жунусова, – с 2008 года работает по европейским стандартам. А в 2015 году мы получили сертификат EDQM – европейского директората по качеству. То есть прошли аккредитацию, которую подтверждаем ежегодно в Европейском союзе. Теперь в планах дальнейшее продвижение в этом направлении. В 2018 году хотим подать заявку на расширение области аккредитации в части биологических испытаний и испытаний медицинских изделий. Для этого у нас имеются все виды лабораторий: иммунобиологическая, микробиологическая и токсикологическая, виварий, лаборатория испытаний медицинских изделий, отдел по обслуживанию лабораторного оборудования. Ну а по физико-химическим испытаниям аккредитацию мы прошли.
– Гражданам, – продолжает заместитель генерального директора НЦЭЛС Акмарал КАБДЕНОВА, – которые переживают за качество препаратов, имеющихся на нашем фармацевтическом рынке, мы бы хотели сказать: сейчас у нас есть все условия, чтобы проверить их при допуске на рынок. Есть лаборатории, которые оснащены по последнему слову техники. И в этом году мы ожидаем их дооснащение. Мы проводим более 2 000 видов различных испытаний. Для этого у нас есть высокоэффективные жидкостные газовые хроматографы, спектрометры, спектрофотометры, потенциометры, атомно-абсорбционные спектрометры, которые позволяют контролировать металлы. Фармацевтическая продукция проверяется на соответствие с требованиями нормативного документа по качеству не только при допуске на рынок, но и в пострегистрационный период, когда завозится либо производится отечественными производителями каждая новая партия или серия товара. Этим у нас занимаются 90 специалистов только в одном нашем головном испытательном центре. А еще у нас 8 филиалов в регионах: Караганде, Костанае, Астане, Павлодаре и других городах.
Как обнаружить фальсификат?
– Прежде чем центр прошел такую важную аккредитацию в Европейском союзе, – говорит Акмарал Кабденова, – мы подготовили в нем все системы жизнеобеспечения: воздуховоды, фильтры, оборудование, расходные материалы, реактивы. Постоянно проводим тренинги с персоналом. Потому все, что зарегистрировано в реестре лекарственных препаратов в Казахстане, проверено в соответствии с требованиями законодательства нашей республики, с Кодексом о здоровье народа и системе здравоохранения.
Все случаи побочного действия лекарственных средств мы отслеживаем по всем регионам. И любой человек, который зашел в аптеку, может проверить, был ли проверен тот или иной лекарственный препарат, по наличию его в реестре и по заключению о его безопасности и качеству. Там же указано, на какую его серию выдано заключение. Так можно выявить любой фальсификат.
– Что означает получение сертификата по качеству Европейского союза?
– Не во всех странах бывшего СНГ есть такие аккредитованные лаборатории. Есть они в России и Беларуси, но нет их в Киргизии и Армении. В этом году мы проходим еще и преквалификацию лабораторий Всемирной организации здравоохранения.
А при сотрудничестве со странами Евразийского экономического союза это будет означать нашу конкурентоспособность в том плане, что мы можем быть так называемым референтным государством. Регистрация лекарственного средства того или иного производителя в таком государстве будет означать признание ее сразу во всей пятерке стран ЕАЭС. То есть и в Казахстане, и в России, Беларуси, Армении и Киргизии.
Более того, наш Национальный центр в рамках ЕАЭС был выбран в качестве разработчика правил экспертизы лекарственных средств и медицинских изделий, а также правил их допуска на рынок. С этим мы успешно справились и теперь выступаем с нашими презентациями и в Евразийском, и в Европейском союзе.
Алматы
Оставить комментарий
Оставлять комментарии могут только зарегистрированные пользователи